
En esta primera parte, les hablaré sobre la termodinámica clásica asociada a sustancias puras y sin reacciones químicas. También se supondrá la existencia del equilibrio y la existencia de procesos reversibles (que definiremos más adelante).
Ahora hablemos de definiciones básicas.

Es toda sustancia que conforma parte del universo material. Posee una masa y ocupa cierto espacio. En la naturaleza pueden existir 3 fases: líquido, sólido o gaseoso. Todo la materia esta conformado por átomos, los cuales se asocian en grupos específicos llamados moléculas los cuales tienen propiedades físicas y químicas propias de cada molécula.

Es la medida de la cantidad de materia en un cuerpo. La masa de un cuerpo es constante sin importar si cambia su estado físico (sólido, líquido o gaseoso). También se mantiene constante incluso al sufrir una reacción química, lo cual implica únicamente un reordenamiento en la organización de los átomos ( se rompen unas moléculas y se forman otras nuevas). Pero la cantidad de átomos individuales Siempre es el mismo.

Es la fuerza que ejerce la gravedad sobre un objeto (que tiene masa)
Peso es igual a masa por gravedad, es decir, la masa es constante pero el peso cambia en función del lugar del universo ya que la gravedad es diferente.

Generalmente se confunde el uso de los términos masa y peso pero es clara la distinción .

Este puede ser uno de los conceptos más complejos ya que es una definición de un base arbitraria. El mol como la docena es una unidad que cuenta con una cantidad fija de objetos. Una docena son doce objetos del mismo tipo. El mol cuenta específicamente átomos, la definición formal esta ligada al numero de avogadro el cual es la definición de la "docena de átomos"
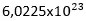 átomos
átomosSe determina experimentalmente como la cantidad de átomos contenida en 12 gr de Carbono12.
Finalmente un mol de una sustancia para cualquiera (átomos o moléculas) son exactamente
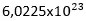 átomos de esa sustancia.
átomos de esa sustancia.

Es la masa correspondiente a un mol de una sustancia dada cualquiera.
Ejemplo

Finalmente la masa molecular de una sustancia se reporta como sigue:
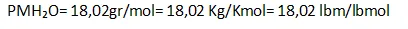
Como pueden observar los números no se modifican , lo que cambia es el sistema de unidades, mas adelante lo explicaremos.
Los conceptos básicos abarcan una amplia gama de definiciones, por ahora los dejaremos hasta aquí, y volveré pronto para seguir enseñando y prendiendo con uds.